연구동향
“약물에 CH3 group 대신에 CD3 group 도입을 고려해 보세요.” (Deuterated Drug 개발현황)
작성자
관리자
작성일
2022-11-04 13:59
조회
1447
화학적으로 탄소-수소 (C-H bond) 결합보다 탄소-중수소(C-D bond) 결합이 강하기 때문에 C-D 결합이 포함된 약물은 체내에서 산화적 대사(oxidative metabolism)반응속도가 느려져 약물의 half-life가 증가되고 toxic metabolite 생성이 감소하여 PK 및 safety profile이 개선될 수 있다 (deuterium-induced “metabolic shunting”).
이러한 이론에 근거하여 수소(H, hydrogen) 대신에 중수소(D, deuterium)를 도입한 deuterated drug의 개발이 1970년대 이후 활발하게 진행되고 있다. 최근에는 deuterated 화합물 및 약물을 전문적으로 연구하는 회사도 다수 생겨났다 (e.g., Concert Pharmaceuticals, Deuteria Pharmaceuticals, DeuteRx, Protia, Auspex, Retrotope).
또한 최근 FDA에서는 deuterated drug 개발에 있어서 undeuterated parent drug 데이터의 활용을 허가하여 deuterated drug 개발을 촉진하기도 하였다 (Hybrid regulatory pathway (505(b)(2)).
Deuterium (D)이 도입된 deuterated drug의 개발에는 크게 두 가지 방법이 있다.
(1) deuterium switch : 기존 약물의 구조에서 hydrogen을 deuterium으로 치환(swapping) 하거나,
(2) de novo 합성 : 초기 약물 디자인에서부터 deuterium을 포함하여 개발을 진행하는 방법이 있다.
현재 FDA 승인을 받았거나 활발하게 개발이 진행되고 있는 deuterated drug의 현황에 대하여 소개 한다.
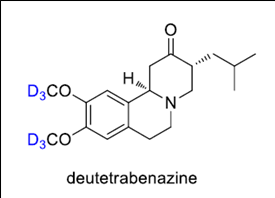
Austedo(deutetrabenazine)는 Huntington’s disease-related movement disorders의 치료제로 2008년 FDA 승인된 Xenazine(tetrabenazine)의 화학구조에서 2개의 CH3 group을 CD3 group으로 변경한 약물이다. Deutetrabenazine은 Tetrabenazine에 비하여 개선된 half-life (twice vs. three times daily doses) 와 side effect profile (reduced sleepiness, depression and anxiety)을 보여주었다.
잘 알려진 당뇨병 치료제인 Pioglitazone(Actos)은 off-label로 비알콜성지방간염 (NASH, nonalcoholic steatohepatitis) 치료제로도 사용 되지만 부작용이 심하여 많이 사용되지는 않는다. Pioglitazone은 (R)- 과 (S)-isomer의 2가지 입체이성질체로 존재하지만 in vitro & in vivo에서 쉽게 epimerization이 일어나기 때문에 실제로는 (R), (S)-혼합물인 racemic 형태로 판매되고 있다. Deuterium-Enriched Chiral Switching 전문회사인 DeuteRx는 pioglitazone의 화학구조에서 chiral center에 있는 수소를 deuterium으로 치환하면 (R)- 과 (S)-isomer가 쉽게 분리할 수 있고 분리된 후 서로 epimerization도 일어나지 않는다는 것을 발견하였다. 각각의 deuterated isomer를 사용하여 NASH에 대하여 생체실험을 한 결과 (R)-isomer가 약효가 높고 (S)-isomer에 의한 독성(PPAR-gamma효과)도 없는 것으로 밝혀졌다.
Deuterium-Stabilized (R)-Pioglitazone (PXL065)은 Poxel사에 기술이전되어 현재 NASH에 대하여 임상 2상시험을 진행중이며 최근 긍정적인 시험결과를 발표하였다.
이외에도 현재 개발중인 deuterium-switched drug으로는 AVP-786(d6-dextromethorphan, Phase III), ALK-001(d3-vitamin A, Phase III), RT001(d2-linoleic acid ethyl ester, Phase II) 등이 있다. (아래 표 참조)
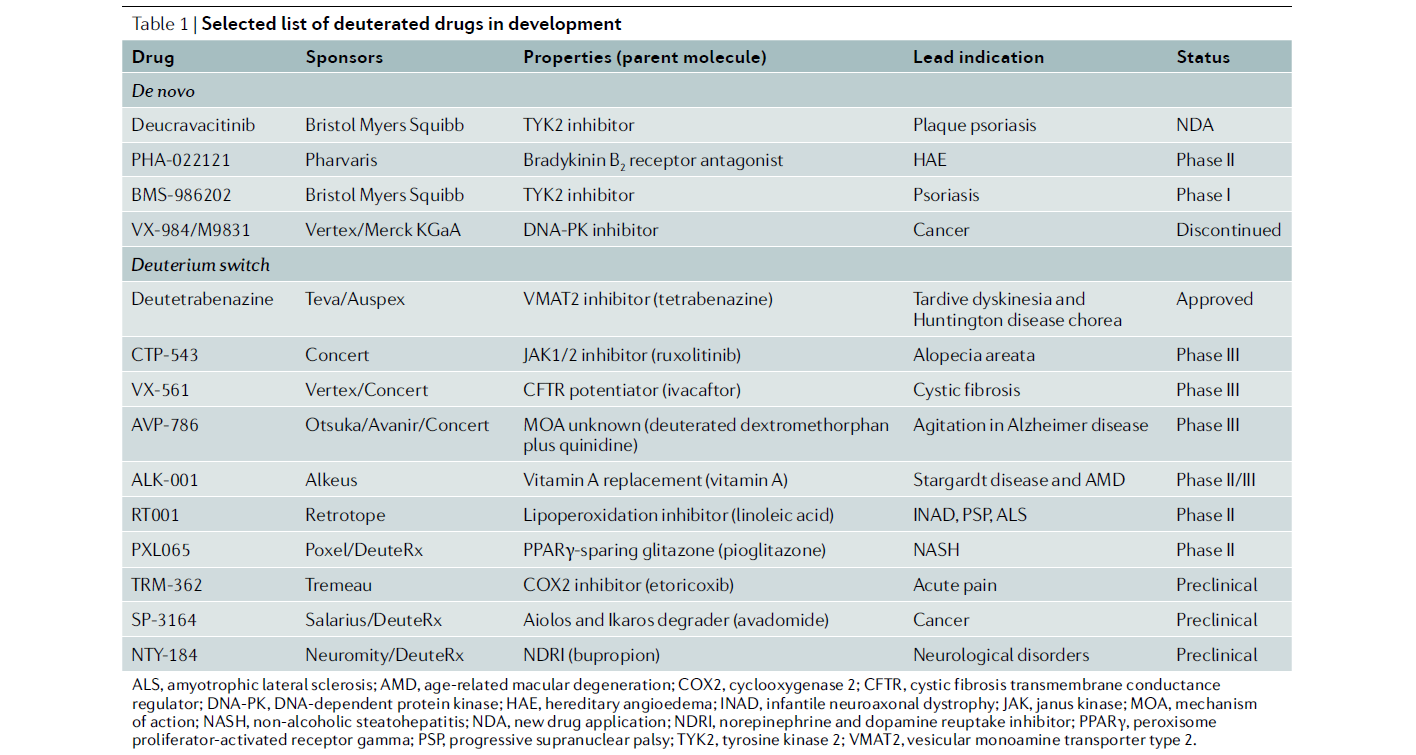
현재 개발중인 de novo deuterated drug은 deuterium-switched drug에 비하여 많이 보고되어 있지 않다. Bristol Myers Squibb에서 psoriasis에 대하여 임상 1상시험을 진행중인 BMS-986202는 올해 FDA 승인을 받은 deucravacitinib(Sotyktu)의 back-up 화합물이다.
Deuterated drug은 PK 및 safety profile이 개선된 old drug의 revitalization 수단으로 또는 기존 약물의 특허연장 및 회피 수단으로 활용되기도 한다. 그러나 최근에는 제삼자의 deuterated version 특허출원을 방지하기 위하여 신약특허에 선제적으로 deuterated version을 포함시키는 경우도 증가하고 있다. 어쨌든 중수소(deuterium)을 포함하는 신약의 개발이 점점 증가하고 있다. Fluorine이 포함된 약물이 1970년대에는 2% 이하였으나 오늘날에는 FDA 승인약물의 25% 나 차지하고 있는 것처럼 말이다.
Nature Review Drug Discovery, volume 21, September 2022, 623.
First de novo deuterated drug poised for approval
Nature Biotechnology volume 35, pages 493–494 (2017)
First deuterated drug approved
Nature Reviews Drug Discovery volume 15, pages219–221 (2016)
Deuterated drugs draw heavier backing
J. Med. Chem. 2019, 62, 5276−5297
Applications of Deuterium in Medicinal Chemistry
이러한 이론에 근거하여 수소(H, hydrogen) 대신에 중수소(D, deuterium)를 도입한 deuterated drug의 개발이 1970년대 이후 활발하게 진행되고 있다. 최근에는 deuterated 화합물 및 약물을 전문적으로 연구하는 회사도 다수 생겨났다 (e.g., Concert Pharmaceuticals, Deuteria Pharmaceuticals, DeuteRx, Protia, Auspex, Retrotope).
또한 최근 FDA에서는 deuterated drug 개발에 있어서 undeuterated parent drug 데이터의 활용을 허가하여 deuterated drug 개발을 촉진하기도 하였다 (Hybrid regulatory pathway (505(b)(2)).
Deuterium (D)이 도입된 deuterated drug의 개발에는 크게 두 가지 방법이 있다.
(1) deuterium switch : 기존 약물의 구조에서 hydrogen을 deuterium으로 치환(swapping) 하거나,
(2) de novo 합성 : 초기 약물 디자인에서부터 deuterium을 포함하여 개발을 진행하는 방법이 있다.
현재 FDA 승인을 받았거나 활발하게 개발이 진행되고 있는 deuterated drug의 현황에 대하여 소개 한다.
<1> Deuterium-switched drug
Austedo(deutetrabenazine, d6-tetrabenazine)
최초로 FDA 승인을 받은 deuterated drug은 Teva Pharmaceutical의 Austedo(deutetrabenazine)이다. VMAT2(vesicular amine transporter 2) inhibitor인 Austedo는 Huntington’s disease-related movement disorders의 치료제로 임상시험에서 효능과 안전성이 undeuterated counterpart 보다 우수하다는 것이 입증되어 2017년 FDA의 승인을 받았다. 많은 사람들이 특히 deuterium이 포함된 약물의 safety에 대하여 높은 관심을 가졌지만 임상시험결과 safety profile이 더 개선된 것으로 나타났다.Austedo(deutetrabenazine)는 Huntington’s disease-related movement disorders의 치료제로 2008년 FDA 승인된 Xenazine(tetrabenazine)의 화학구조에서 2개의 CH3 group을 CD3 group으로 변경한 약물이다. Deutetrabenazine은 Tetrabenazine에 비하여 개선된 half-life (twice vs. three times daily doses) 와 side effect profile (reduced sleepiness, depression and anxiety)을 보여주었다.

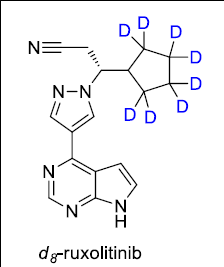
CTD-543(Deuruxolitinib, d8-ruxolitinib)
2023년 초에 FDA의 승인을 받을 것으로 예상되고 있는 deuterium-switched drug은 Concert Pharmaceutical의 JAK1/2 inhibitor인 CTD-543(d8-ruxolitinib, Deuruxolitinib) 이다. Deuruxolitinib의 적응증(indication)은 autoimmune에 의한 탈모(alopecia areata) 치료이다. Deuruxolitinib은 Incyte에서 개발되어 myelofibrosis 치료제로 2011년에 FDA 승인을 받은 JAK1/2 inhibitor인 Jakafi(ruxolitinib)의 화학구조에서 cyclopentane ring에 있는 8개의 hydrogen이 8개의 deuterium으로 치환된 약물이다. Deuruxolitinib의 1,200명을 대상으로한 임상 3상 시험에서 효능과 safety에서 모두 positive한 결과를 얻었다고 보고되었다. 한편, 본 약제는 Concert와 Incyte 사이에 특허 분쟁이 진행중이다. Incyte 는 조성특허(composition-of-matter patent)를 주장하고 있고 Concert는 용도특허(method-of-use patent)에서 승소한 바 있다.
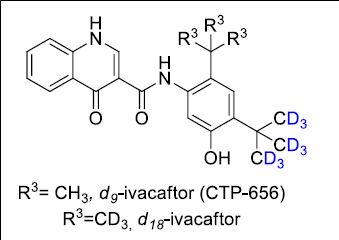
VX-561(CTP-656, d9-ivacaftor)
VX-561(d9-ivacaftor)는 Concert에서 개발하여 2017년 Vertex로 US$ 250 million에 기술이전 되었고 현재 cystic fibrosis에 대하여 임상 3상 시험 중이다. VX-561(d9-ivacaftor)는 cystic fibrosis transmembrane regulator (CFTR) potentiator로 Vertex에서 개발되어 2012년에 FDA 승인받은 ivacaftor의 화학구조에서 하나의 t-Butyl group 9개의 수소가 deuterium으로 치환된 약물이다. 흥미롭게도 original ivacaftor는 Vertex에서 개발되었으나 이의 deuterated version인 VX-561(d9-ivacaftor)는 Concert에서 개발되어 다시 Vertex로 기술이전 되었다.
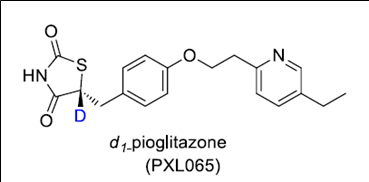
PXL065(d1-(R)-pioglitazone)
일반적인 deuterated drug은 대사속도의 조절에 따른 PK 또는 safety profile을 개선하기 위한 목적으로 개발되지만 PXL065(d1-pioglitazone)은 다른 목적(stereo-isomer의 안정화)을 위하여 개발되었다.잘 알려진 당뇨병 치료제인 Pioglitazone(Actos)은 off-label로 비알콜성지방간염 (NASH, nonalcoholic steatohepatitis) 치료제로도 사용 되지만 부작용이 심하여 많이 사용되지는 않는다. Pioglitazone은 (R)- 과 (S)-isomer의 2가지 입체이성질체로 존재하지만 in vitro & in vivo에서 쉽게 epimerization이 일어나기 때문에 실제로는 (R), (S)-혼합물인 racemic 형태로 판매되고 있다. Deuterium-Enriched Chiral Switching 전문회사인 DeuteRx는 pioglitazone의 화학구조에서 chiral center에 있는 수소를 deuterium으로 치환하면 (R)- 과 (S)-isomer가 쉽게 분리할 수 있고 분리된 후 서로 epimerization도 일어나지 않는다는 것을 발견하였다. 각각의 deuterated isomer를 사용하여 NASH에 대하여 생체실험을 한 결과 (R)-isomer가 약효가 높고 (S)-isomer에 의한 독성(PPAR-gamma효과)도 없는 것으로 밝혀졌다.
Deuterium-Stabilized (R)-Pioglitazone (PXL065)은 Poxel사에 기술이전되어 현재 NASH에 대하여 임상 2상시험을 진행중이며 최근 긍정적인 시험결과를 발표하였다.

이외에도 현재 개발중인 deuterium-switched drug으로는 AVP-786(d6-dextromethorphan, Phase III), ALK-001(d3-vitamin A, Phase III), RT001(d2-linoleic acid ethyl ester, Phase II) 등이 있다. (아래 표 참조)

<2> de novo deuterated drug 개발
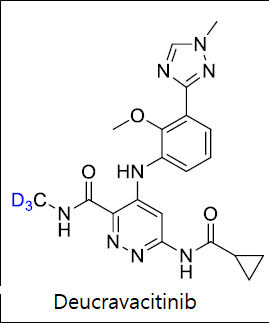
Deucravacitinib(Sotyktu)
TYK2 inhibitor인 Deucravacitinib(Sotyktu)는 moderate to severe psoriasis 적응증(indication)에 대하여 2022년 9월 FDA의 승인을 받았다 (Bristol Myers Squibb). 이 약제는 first-in-class oral, allosteric TYK2 inhibitor로서 JAK1, JAK2, JAK3에 대하여 선택성이 매우 높아 특별한 부작용은 나타내지 않았다고 보고되었다. Deucravacitinib(Sotyktu)은 기존 약물의 화학구조에서 수소원자를 deuterium을 치환한 deuterium-switched drug이 아니고 개발 초기부터 deuterium을 도입하여 개발된 de novo deuterated drug이다. Deucravacitinib 개발자들은 초기에 CH3 group이 도입된 화합물을 만들어서 실험한 결과 CH3 group이 쉽게 대사되어서 non-selective & toxic metabolites가 생성되는 것을 알았고 이를 해결하기 위한 방안으로 CH3 대신 대사가 느리게 진행할 것으로 예상되는 CD3 group을 도입한 화합물을 합성하였다. 실제로 mouse를 사용한 실험을 진행한 결과 CH3 의 경우 3% 였던 non-selective metabolites 생성이 CD3 도입된 화합물의 경우 검출되지 않는다는 것을 확인하였다. Deucravacitinib(Sotyktu)은 1,700명이 참여한 임상 3상 시험에서 대조약제인 Amgene 의 apremilast에 비하여 우수한 효능을 보였으며 일반적으로 JAK inhibitor에서 나타나는 부작용도 보이지 않았다.
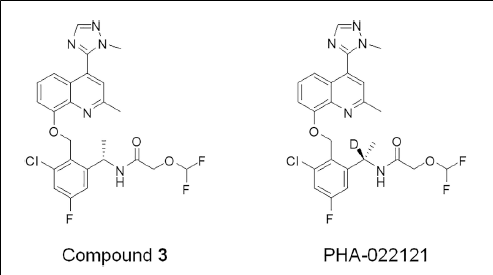
PHA-022121(Deucrictibant)
PHA-022121(Deucrictibant)은 저분자 bradykinin B2 receptor(BK2) antagonist로 hereditary angioedema(HAE) 적응증에 대하여 임상 2상에 있는 화합물이다. Pharvaris의 연구자들은 디자인한 화합물의 SAR 연구를 통하여 먼저 BK2 antagonist로 우수한 효능을 보이는 compound 3을 발굴하였고 나아가 chiral center hydrogen을 deuterium으로 치환한 PHA-022121(Deucrictibant)을 합성하여 in vitro pharmacological profiling 시험결과 알려진 human BK2 antagonist인 icatibant보다 약 20배 높은 효능을 보였다.
현재 개발중인 de novo deuterated drug은 deuterium-switched drug에 비하여 많이 보고되어 있지 않다. Bristol Myers Squibb에서 psoriasis에 대하여 임상 1상시험을 진행중인 BMS-986202는 올해 FDA 승인을 받은 deucravacitinib(Sotyktu)의 back-up 화합물이다.
Deuterated drug은 PK 및 safety profile이 개선된 old drug의 revitalization 수단으로 또는 기존 약물의 특허연장 및 회피 수단으로 활용되기도 한다. 그러나 최근에는 제삼자의 deuterated version 특허출원을 방지하기 위하여 신약특허에 선제적으로 deuterated version을 포함시키는 경우도 증가하고 있다. 어쨌든 중수소(deuterium)을 포함하는 신약의 개발이 점점 증가하고 있다. Fluorine이 포함된 약물이 1970년대에는 2% 이하였으나 오늘날에는 FDA 승인약물의 25% 나 차지하고 있는 것처럼 말이다.
작성 : 이현규 (한국화합물은행)
<관련문헌 바로가기>Nature Review Drug Discovery, volume 21, September 2022, 623.
First de novo deuterated drug poised for approval
Nature Biotechnology volume 35, pages 493–494 (2017)
First deuterated drug approved
Nature Reviews Drug Discovery volume 15, pages219–221 (2016)
Deuterated drugs draw heavier backing
J. Med. Chem. 2019, 62, 5276−5297
Applications of Deuterium in Medicinal Chemistry